大家好,今天小编关注到一个比较有意思的话题,就是关于氯气的制备的问题,于是小编就整理了4个相关介绍氯气的制备的解答,让我们一起看看吧。
制备氯气?
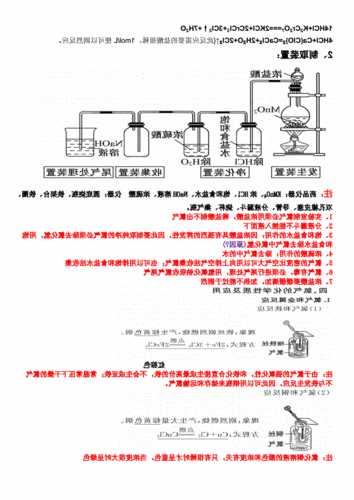
实验室的氯气制备方法:
①用浓HCl和MnO2混合加热制取氯气。
4HCl +MnO2 == MnCl2 + 2H2O +Cl2↑
②高锰酸钾(KMnO4)跟浓盐酸反应制氯气
2KMnO4+16HCl==2KCl+2MnCl2+8H2O+5Cl2↑
③氯酸钾(KClO3)与浓盐酸反应制取氯气
KClO3+6HCl=KCl+3H2O+3Cl2↑
制取氯气的三个方程式?
MnO2 + 4 HCl ==△== MnCl2 + Cl2↑ + 2 H2O2 KMnO4 + 16 HCl = 2 MnCl2 + 5 Cl2↑ + 2 KCl + 8 H2OKClO3 + 6 HCl = KCl + 3 Cl2 + 3 H2O
氯气的制备原理?
实验室的氯气制备方法:
1.用浓盐酸跟二氧化锰混合加热制取氯气。
加热
4HCl + MnO2 == MnCl2 + 2H2O +Cl2↑
2.高锰酸钾跟浓盐酸反应.
2KMnO4+16HCl=2KCl+2MnCl2+8H2O+5Cl2↑
3.氯酸钾与浓盐酸反应.
KClO3+6HCl=KCl+3H2O+3Cl2↑
但考虑到纯度和经济,安全性,制取的效率所以实验室一般用二氧化锰与盐酸反应制备
1.工业生产中用直流电电解饱和食盐水法来制取氯气: 2NaCl+2H2O=电解=H2↑+Cl2↑+2NaOH 2.实验室通常用氧化浓盐酸的方法来制取氯气: 常见的氧化剂有:MnO2、K2Cr2O7(重铬酸钾)、KMnO4、KClO3、Ca(ClO)2 发生的反应分别是: 4HCl(浓)+MnO2=加热=MnCl2+Cl2↑+2H2O
clo的制备?
工业制法
工业生产中用直流电电解饱和食盐水法来制取氯气,其化学方程式为2NaCl+2H2O==(通电)H2↑+Cl2↑+2NaOH,但此法通过电解槽出来的氯气中含有许多杂质,须进行消除杂质或进行干燥处理。
2、实验室制法
实验室通常用氧化浓盐酸的方法来制取氯气,其化学方程式4HCl+Ca(ClO)₂==CaCl₂+2H₂O+2Cl₂↑,此法制备原理为氯离子+氧化剂+酸性环境,氧化剂的氧化性不强的话还需不同程度加热。
Clo(即氯氧化铑)可以通过将氯气通入含有氯化铑酸钠的水溶液中来制备。首先,将氯化铑酸钠溶解在水中形成溶液,然后将氯气缓慢通入溶液中。在反应中,氯气氧化了铑(III)离子成为氯氧化铑(IV)离子,从而生成Clo。制备过程中需要注意控制氯气通入速度和反应温度,以及在安全条件下进行操作。
最后,通过过滤、洗涤和干燥等步骤,可以得到纯净的氯氧化铑。
氯酸制备方法是:将氯酸铵溶于沸水中,把一定量的硫酸和水的混合物缓慢加入,于真空干燥器中浓缩,可制得40%的氯酸溶液,其组成相当于HClO3·7H2O,也可用阳离子交换树脂法制得。
到此,以上就是小编对于氯气的制备的问题就介绍到这了,希望介绍关于氯气的制备的4点解答对大家有用。
本文转载自互联网,如有侵权,联系删除